| 2023 ESMO主席专场 | 吴炅教授:TROPION-Breast01重磅发布,Dato-DXd显著延长PFS,安全性可控! | |||||
|
|||||
|
前言 日前,欧洲肿瘤内科学会(ESMO)年会在西班牙马德里顺利召开。期间Datopotamab deruxtecan(Dato-DXd)在乳腺癌领域的首个关键性III期临床研究TROPION-Breast01(TB-01)荣登主席专场。研究结果显示,Dato-DXd可显著延长内分泌治疗失败的HR+/HER2-晚期乳腺癌患者的无进展生存期(PFS),且治疗相关不良事件(TRAEs)级别较低、安全性可控。TB-01研究的突破性结果彰显了Dato-DXd在乳腺癌治疗领域的巨大潜力。 值此盛会之际,特邀复旦大学附属肿瘤医院吴炅教授分析解读TB-01研究最新数据,帮助我们梳理Dato-DXd在HR+/HER2-晚期乳腺癌中的应用前景。同时也期待Dato-DXd未来在乳腺癌治疗领域再创佳绩,造福更多患者。 Dato-DXd突破内分泌耐药难题 HR+/HER2-是乳腺癌中最常见的亚型,约占所有乳腺癌的65%,尽管内分泌治疗显著改善了这些患者的预后,但仍有25%的HR+/HER2-早期乳腺癌患者会在5年内复发转移1,2。目前HR+/HER2-晚期乳腺癌患者的一线治疗是以内分泌治疗联合CDK4/6抑制剂为主3。虽然CDK4/6抑制剂取得了良好的疗效,不过约有10%的患者存在对CDK4/6抑制剂的原发性耐药,而其余患者多在CDK4/6抑制剂一线治疗的24~28个月后和二线治疗后更短时间内会出现继发性耐药4。目前CDK4/6抑制剂和内分泌治疗失败后的后线治疗选择有限,因此如何有效的治疗这部分患者仍是目前临床工作中的挑战之一。 滋养层细胞表面抗原2(TROP2)是由TACSTD2基因编码的细胞表面糖蛋白,包括乳腺癌、非小细胞肺癌在内的多种实体瘤中均存在TROP2高表达,TROP2目前也是具有广阔前景的泛肿瘤治疗潜力靶点之一5,6。相关研究表明,TROP2参与激活的MAPK和PI3K-AKT等信号通路与CDK4/6抑制剂和内分泌治疗耐药的产生相关5–8。
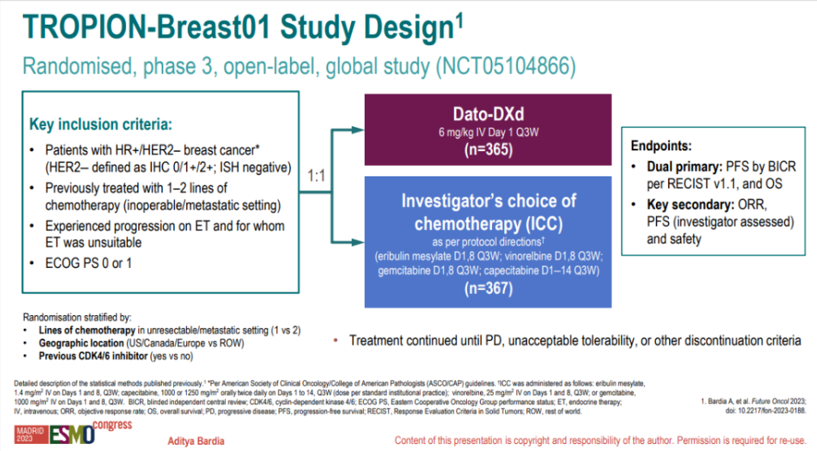
Dato-DXd作为一种新型的TROP2抗体-药物偶联物(ADC),其临床疗效在此前的TROPION-PanTumor01(TP-01)研究中已得到初步证实,在CDK4/6抑制剂和内分泌治疗耐药的HR+/HER2-晚期乳腺癌中具有明确抗肿瘤效果和可控的安全性,III期临床研究TB-01在更大患者群体中进一步验证该药的治疗效果及安全性,研究结果一直备受期待8。 TB-01数据发布,Dato-DXd疗效优越、安全可控 TB-01研究是一项全球多中心、随机、开放标签的III期临床研究,其研究设计如下:
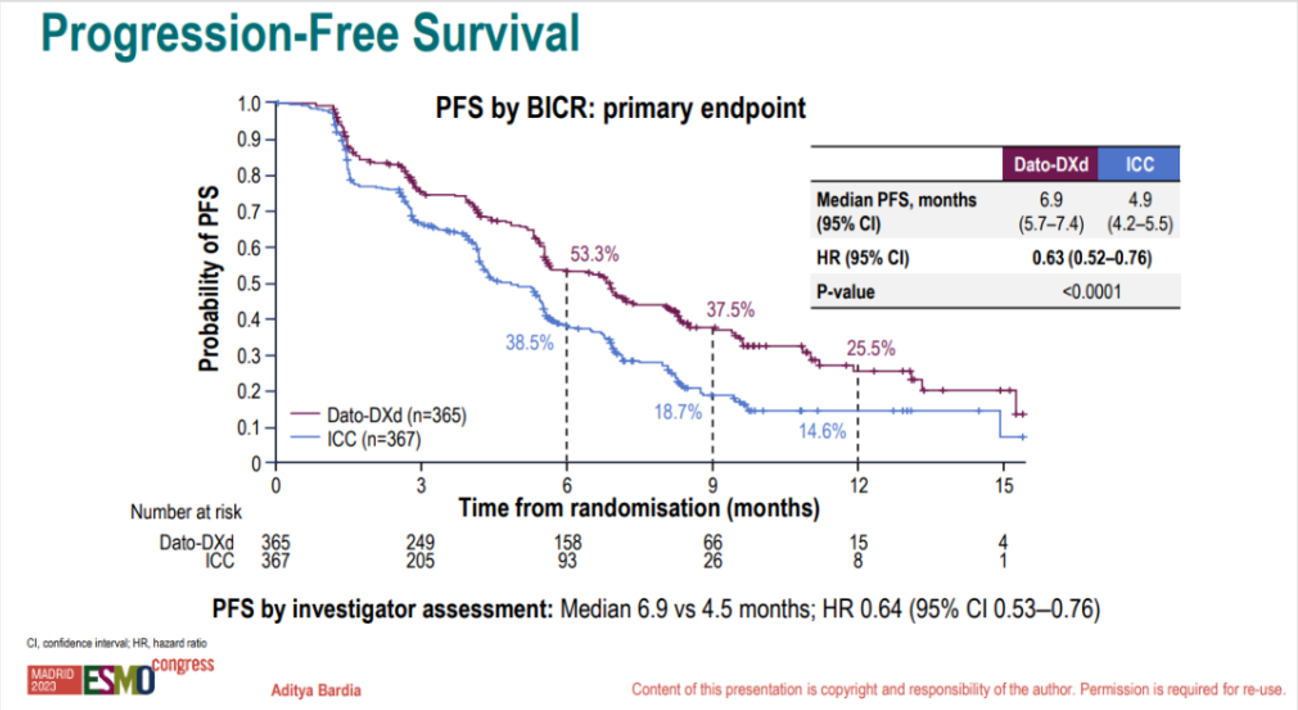
图1 TB-01研究设计 本次大会披露的数据显示,TB-01研究已达PFS主要终点,目前中位随访时间10.8个月,Dato-DXd组患者中位PFS显著优于ICC组(6.9个月 vs 4.9个月;HR=0.63;95%CI 0.52-0.76;p<0.0001)。Dato-DXd组在6个月和9个月的PFS率分别为53.3%(95%CI 47.7-58.5)和37.5%(95%CI 31.9-43.2),高于ICC组的38.5%(95%CI 32.8-44.1)和18.7%(95%CI 13.8-24.3)。
图2 BICR评估的总人群PFS
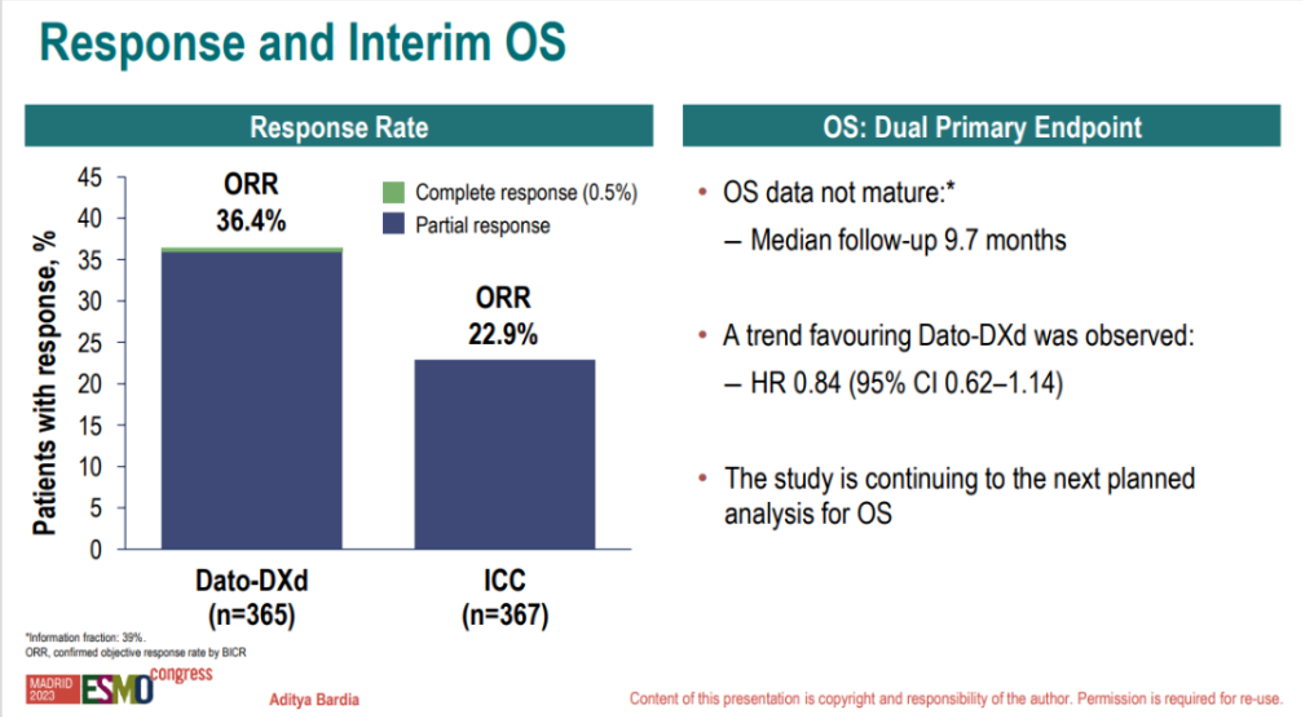
在ORR上,Dato-DXd组也获得了优势,达36.4%(n=133),ICC组仅为22.9%(n=84)。OS数据尚未成熟,但观察到有利于Dato-DXd的趋势(HR=0.84;95%CI 0.62–1.14)。
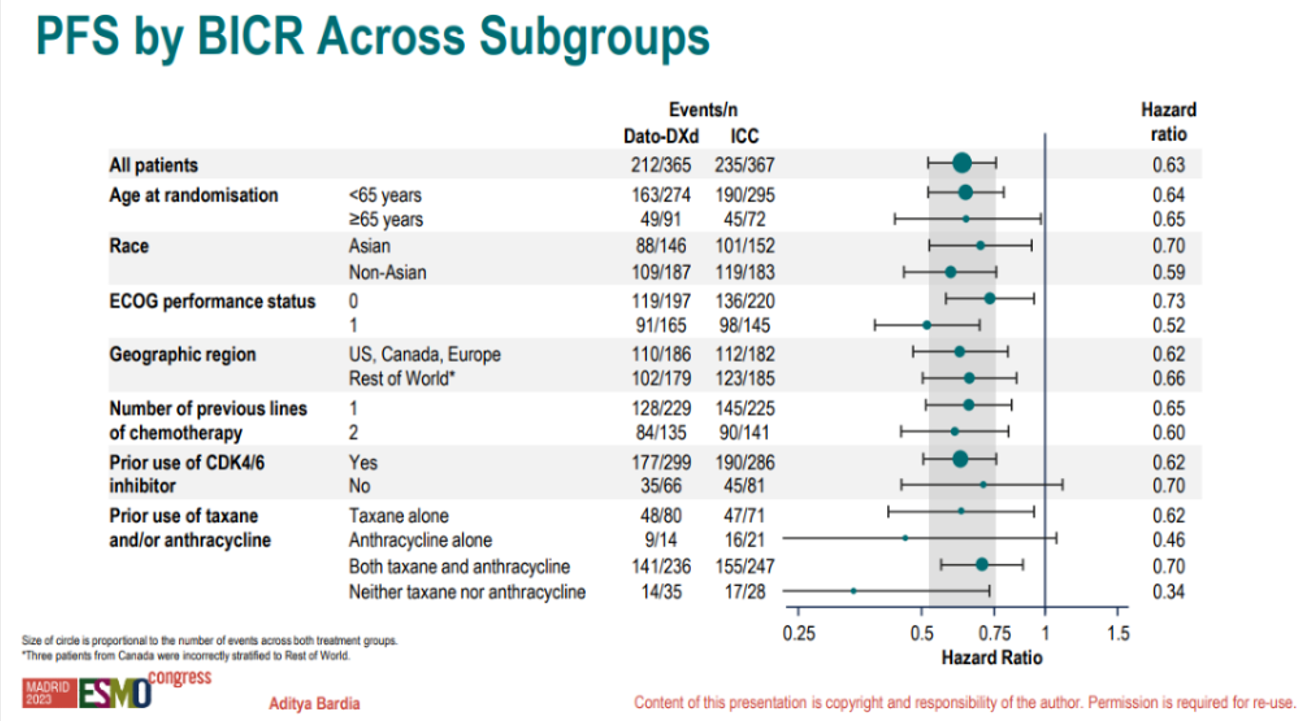
图3 总人群ORR 该研究亚组分析显示,Dato-DXd组和ICC组分别有82%(n=299/365)和78%(n=286/367)的患者既往接受过CDK4/6抑制剂治疗。结果表明,Dato-DXd在CDK4/6经治人群中,显示出了与总人群相似的PFS获益(HR=0.62)。
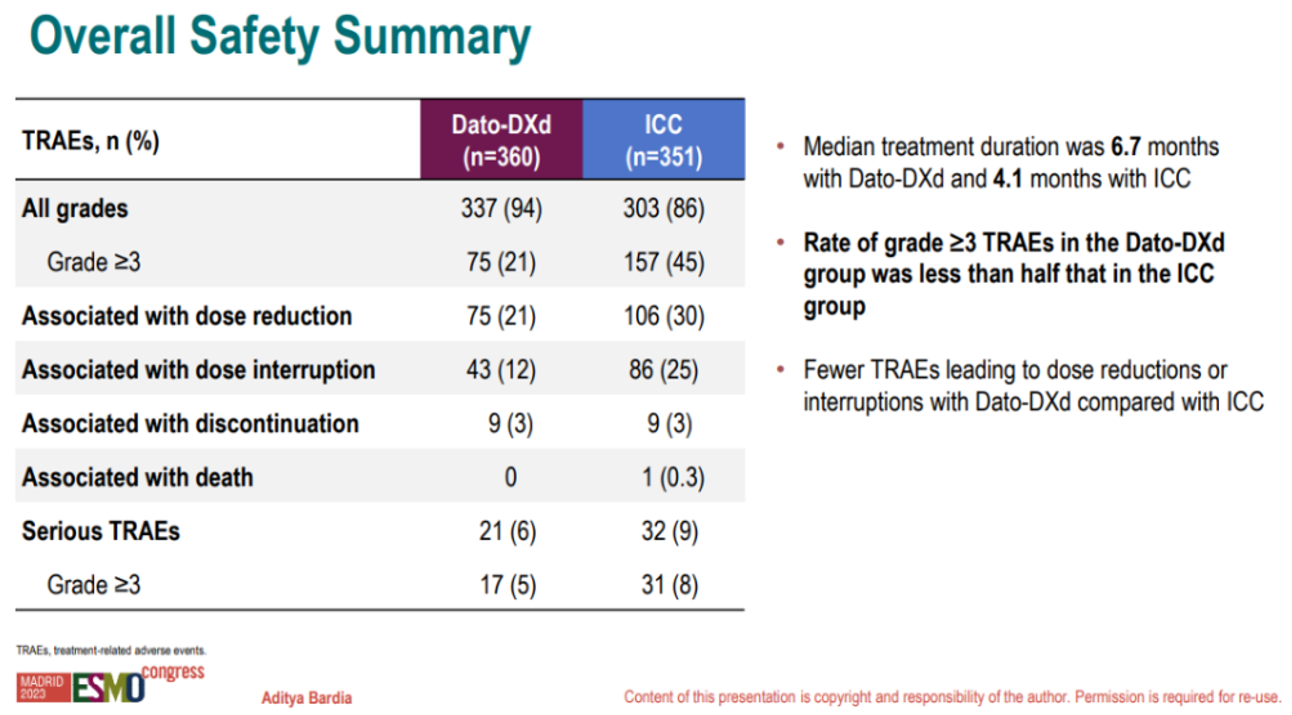
表1 TB-01亚组分析 在安全性上,Dato-DXd组的中位治疗时间为6.7个月,ICC组为4.1个月。虽然Dato-DXd组TRAEs发生率数值上略高(94% vs 86%),但其≥3级TRAEs发生率(21% vs 45%)和因TRAEs导致的剂量下调(21% vs 30%)或治疗中断(12% vs 25%)的比例较ICC组更低。
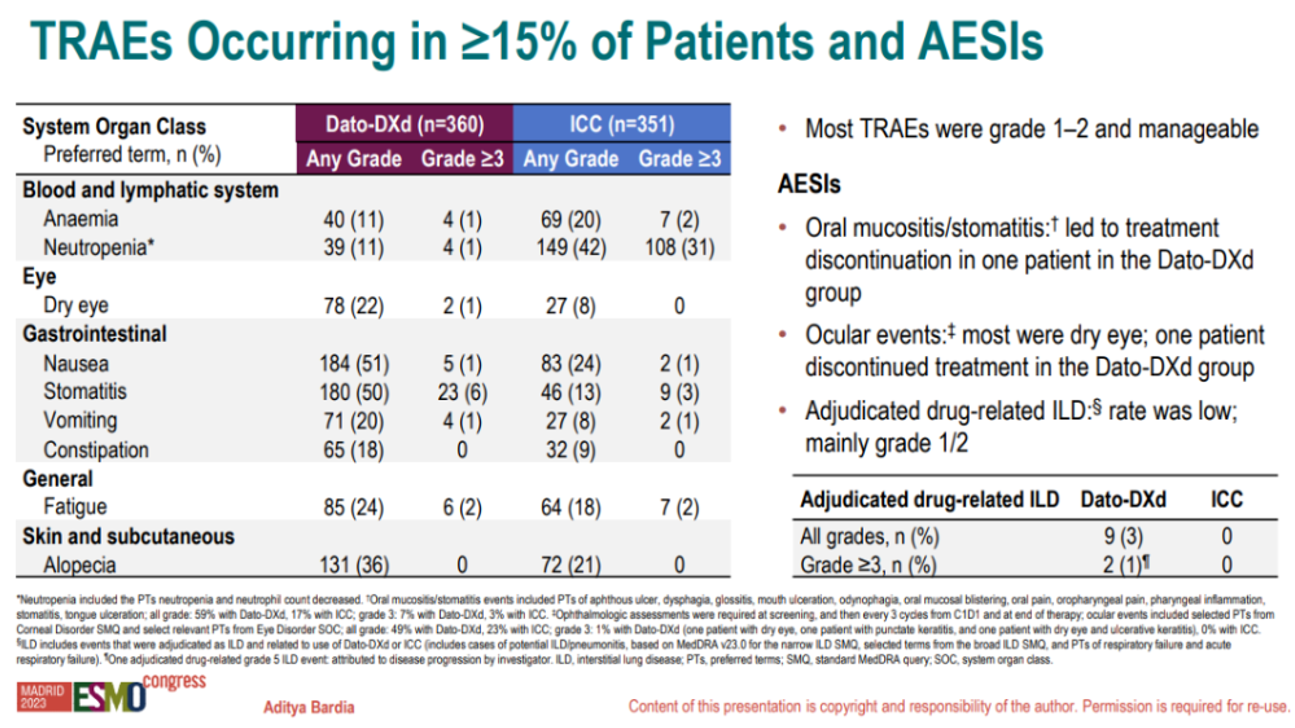
表2 TB-01安全性分析 Dato-DXd治疗患者中最常见的TRAEs为恶心(51%)和口腔炎(50%),多为1~2级,≥3级的恶心和口腔炎发生率仅为1%和6%。
表3 TB01安全性分析 总体而言,Dato-DXd可有效延长内分泌治疗耐药的HR+/HER2-晚期乳腺癌患者PFS,且亚组分析结果提示,在82%既往接受过CDK4/6抑制剂治疗的患者中,Dato-DXd也表现出非常优秀的抗肿瘤效果。同时Dato-DXd治疗的TRAEs也通常为低级别且易管理,整体安全性可控,患者耐受性较好。 此前,TROP2 ADC戈沙妥珠单抗(SG)基于TROPiCS-02研究已获FDA批准用于HR+/HER2-晚期乳腺癌的后线治疗。Dato-DXd作为后起之秀,已展现出优异的疗效,且安全性方面更具优势。TB-01研究中Dato-DXd治疗患者≥3级TRAEs发生率仅为21%,远低于SG在TROPiCS-02研究中的74%;并且SG治疗期间患者可能发生重度甚至危及生命的中性粒细胞减少,SG所有级别和≥3级中性粒细胞减少的发生率分别为70%和51%,而Dato-DXd仅为11%和1%。由此可见与SG相比,Dato-DXd展现出了更加可控的安全性,为HR+/HER2-晚期乳腺癌患者CDK4/6抑制剂耐药人群提供了更多的治疗选择。DESTINY-Breast04(DB-04)研究结果提示,德曲妥珠单抗(T-DXd)在HR+/HER2-low患者中取得的优异疗效。对于既往内分泌治疗和CDK4/6治疗耐药且已接受化疗后进展的HR+/HER2-患者,可根据其HER2表达情况进行分类而治。ADC的迅速发展也为我们临床带来新的问题,如精准选择更优获益ADC药物、ADC药物之间排布以及用药管理等。 Dato-DXd全面布局HER2-乳腺癌 TB-01的突破性结果提示我们,Dato-DXd是HR+/HER2-晚期乳腺癌内分泌治疗失败后的更有效且更安全的治疗选择。除此之外,Dato-DXd联合免疫治疗在晚期三阴性乳腺癌(TNBC)中也有令人满意的表现。本次大会上BEGONIA研究公布的最新结果表明,Dato-DXd联合度伐利尤单抗晚期一线治疗TNBC的PFS达13.8个月,ORR为79%。这一优异结果不仅为晚期TNBC患者提供了新的治疗选择,也展现出了Dato-DXd联合免疫治疗在乳腺癌领域中广阔的治疗前景。 据悉,目前Dato-DXd在乳腺癌领域还有两项III期临床研究正在进行,分别是Dato-DXd单药晚期一线治疗TNBC的TROPION-Breast02研究和辅助强化治疗TNBC的TROPION-Breast03研究。随着Dato-DXd在乳腺癌领域崭露头角,由衷期待TB-01的后续随访数据以及TROPION-Breast02和TROPION-Breast03的研究结果能够为临床决策提供更充分的循证医学证据,为乳腺癌患者带来治疗获益。
参考文献: 1.West MT, Goodyear SM, Hobbs EA, et al. Real-World Evaluation of Disease Progression After CDK 4/6 Inhibitor Therapy in Patients With Hormone Receptor-Positive Metastatic Breast Cancer. Oncologist. 2023;28(8):682-690. 2.Marios C, Papadimitriou a, Anastasia Pazaiti b, et al. Mechanisms and strategies to overcome a therapeutic problem in the treatment of hormone receptor-positive metastatic breast cancer. Biochim Biophys Acta Mol Cell Res. 2022 Dec;1869(12):119346. 3.Lopez-Tarruella S, Echavarria I, Jerez Y, Herrero B, Gamez S, Martin M. How we treat HR-positive, HER2-negative early breast cancer. Future Oncology. 2022;18(8):1003-1022. 4.Lee JS, Hackbart H, Cui X, et al. CDK4/6 Inhibitor Resistance in Hormone Receptor-Positive Metastatic Breast Cancer: Translational Research, Clinical Trials, and Future Directions. Int J Mol Sci. 2023 Jul 22;24(14):11791. 5.Okajima D, Yasuda S, Maejima T, et al. Datopotamab Deruxtecan, a Novel TROP2-directed Antibody–drug Conjugate, Demonstrates Potent Antitumor Activity by Efficient Drug Delivery to Tumor Cells. Mol Cancer Ther. 2021;20(12):2329-2340. 6.Vidula N, Yau C, Rugo H. Trophoblast Cell Surface Antigen 2 gene (TACSTD2) expression in primary breast cancer. Breast Cancer Res Treat. 2022;194(3):569-575. 7.Gomes I, Abreu C, Costa L, Casimiro S. The Evolving Pathways of the Efficacy of and Resistance to CDK4/6 Inhibitors in Breast Cancer. Cancers (Basel). 2023;15(19):4835. 8.Bardia A, Jhaveri K, Kalinsky K, et al. TROPION-Breast01: Datopotamab deruxtecan vs chemotherapy in pre-treated inoperable or metastatic HR+/HER2- breast cancer. Future Oncol. Published online June 30, 2023. 9.Simon J, Chaix M, Billa O, et al. Survival in patients with HR+/HER2− metastatic breast cancer treated with initial endocrine therapy versus initial chemotherapy. A French population-based study. Br J Cancer. 2020;123(7):1071-1077. 10.Huppert LA, Gumusay O, Idossa D, Rugo HS. Systemic therapy for hormone receptor‐positive/human epidermal growth factor receptor 2‐negative early stage and metastatic breast cancer. CA A Cancer J Clinicians. 2023;73(5):480-515. 11.Laface C, Giuliani F, Melaccio A, et al. The Treatment Landscape of Elderly Patients with Hormone Receptor-Positive Her2 Negative Advanced Breast Cancer: Current Perspectives and Future Directions. J Clin Med. 2023;12(18):6012. |
|||||